सल्फ्यूरिक एसिड की गुणधर्म

प्रत्येक व्यक्ति ने रसायन विज्ञान सबक पर एसिड का अध्ययन किया। इसे उनसे सल्फरिक एसिड कहा जाता है और उन्हें एनएसओ द्वारा नामित किया जाता है4। हमारे सल्फ्यूरिक एसिड गुणों के बारे में, हमारे लेख बताएंगे।
सल्फ्यूरिक एसिड का भौतिक गुण
शुद्ध सल्फ्यूरिक एसिड या मोनोहाइड्रेट हैएक रंगहीन तेल द्रव्य जो एक क्रिस्टलीय द्रव्यमान में + 10 डिग्री सेल्सियस के तापमान पर ठोस बनाता है सल्फ्यूरिक एसिड, प्रतिक्रियाओं के लिए इरादा, 95% एच शामिल हैं2अतः4 और इसकी 1.84 ग्राम / सेमी घनत्व है3। ऐसे एसिड का 1 लीटर का वजन 2 किलोग्राम होता है एसिड इलाज -20 डिग्री सेल्सियस पर संलयन की गर्मी 10.5 केजे / मॉल 10.37 डिग्री सेल्सियस के तापमान पर है
केंद्रित सल्फ्यूरिक एसिड के गुणविविध। उदाहरण के लिए, जब यह एसिड पानी में भंग हो जाता है, तो हाइड्रेट्स के गठन के कारण बड़ी मात्रा में गर्मी (19 किलो कैलोरी / मॉल) जारी की जाएगी। इन हाइड्रेट को ठोस रूप में कम तापमान पर समाधान से पृथक किया जा सकता है।
सल्फ्यूरिक एसिड सबसे बुनियादी में से एक हैरासायनिक उद्योग में उत्पादों यह खनिज उर्वरकों (अमोनियम सल्फेट, सुपरफॉस्फेट), लवण और एसिड, डिटर्जेंट और दवाइयां, कृत्रिम फाइबर, रंजक और विस्फोटक के विभिन्न प्रकार के उत्पादन के लिए है। इसके अलावा, सल्फ्यूरिक एसिड धातु विज्ञान में अनुप्रयोगों (उदाहरण के लिए, यूरेनियम अयस्क का अपघटन), पेट्रोलियम उत्पादों की सफाई के लिए, गैसों को सुखाने के लिए और इतने पर।
सल्फ्यूरिक एसिड के रासायनिक गुण
सल्फरिक एसिड के रासायनिक गुण हैं:
- धातुओं के साथ बातचीत:
- पतला एसिड केवल उन धातुओं को घुलित करता है जो तनाव की एक श्रृंखला में हाइड्रोजन की बाईं ओर खड़े हैं, उदाहरण के लिए एच2+1अतः4+ जेडएन0 = एच2O + Zn+2अतः4;
- सल्फ्यूरिक एसिड के ऑक्सीकरण गुणों में बड़े हैं। जब विभिन्न धातुओं (पीटी, एयू को छोड़कर) के साथ बातचीत करते हैं, तो इसे एच तक घटाया जा सकता है2एस-2 , एस4हे2 या एस0, उदाहरण के लिए:
- 2H2+6अतः4 + 2 एग0 = एस4हे2 + एजी2+1अतः4 + 2 एच2हे;
- 5H2+6अतः4 + 8 ना0 = एच2एस-2 + 4 नो2+1अतः4 + 4 एच2हे;
- केंद्रित एसिड एच2एस+6हे4यह भी कुछ गैर-धातुओं के साथ प्रतिक्रिया करता है (इस प्रकार गरम होता है), इस प्रकार एक निम्न ऑक्सीकरण राज्य के साथ सल्फर यौगिकों में बदल जाता है, उदाहरण के लिए:
- 2H2एस+6हे4 + सी0 = 2 एस4हे2 + सी4हे2 + 2 एच2हे;
- 2H2एस+6हे4 + एस0 = 3 एस4हे2 + 2 एच2हे;
- 5H2एस+6हे4 + 2 पी0 = 2 एच3पी5हे4 + 5 एस4हे2 + 2 एच2हे;
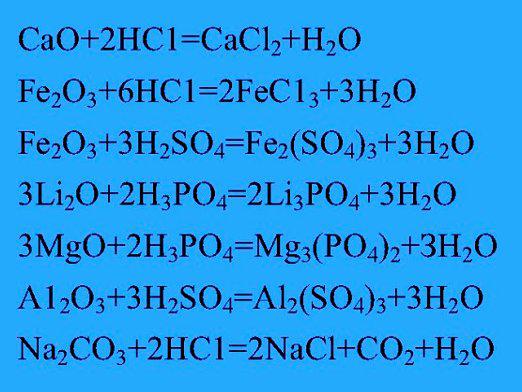
- बुनियादी आक्साइड के साथ:
- एच2अतः4 + क्यूओ = कूसो4 + एच2हे;
- हाइड्रोक्साइड के साथ:
- घन (ओएच)2 + एच2अतः4 = कूसो4 + 2 एच2हे;
- 2 एनएओएच + एच2अतः4 = ना2अतः4 + 2 एच2हे;
- विनिमय प्रतिक्रियाओं के दौरान लवण के साथ बातचीत:
- एच2अतः4 + BaCl2 = 2 एचसीएल + बासो 24;
BaSO का गठन4 (सफेद एसिड में अघुलनशील तलछट) एसिड और घुलनशील sulphates निर्धारित करने के लिए इस्तेमाल किया।
मोनोहाइड्रेट एक आयनिंग विलायक है जिसमें एक अम्लीय पात्र होता है। उदाहरण के लिए, कई धातुओं के सल्फेट को भंग करना बहुत अच्छा है:
- 2H2अतः4 + एचएनओ3 = नहीं2+ + एच3हे+ + 2 एचएसओ4-;
- HClO4 + एच2अतः4 = क्लॉ4- + एच3अतः4+.
केंद्रित एसिड एक काफी मजबूत ऑक्सीडेंट है, खासकर जब गरम होता है, उदाहरण के लिए 2 एच2अतः4 + घन = SO2ए। CuSO4 + एच2ओ
एक ऑक्सीकरण, सल्फर एसिड के रूप में अभिनय, आम तौर पर पहले तो ठीक हो2लेकिन वह notbe लौटी और करने के लिए एस और यहां तक कि ज2एस, उदाहरण के लिए एच2S H2अतः4 = तो2 + 2 एच2ओ एस.
Monogidratpochti एक बिजली का करंट नहीं mozhetprovodit ।और, इसके विपरीत, एसिड के जलीय समाधान अच्छे कंडक्टर हैं । सल्फर एसिड अवशोषणनमी, तो अपनी ispolzujutdlja विभिन्न गैसों के सूखने. एक जलशुष्कक के रूप में, सल्फर एसिड कृत्योंजल वाष्प दबाव का उसका समाधान जब तक गाजा में अपने दबाव से कम है, जो गायब है ।
यदि आप इसे से पतला rastvorsernoj एसिड अब फोड़ा, पानी उबलते बिंदु के साथ होगा३३७ डिग्री सेल्सियस के लिए वृद्धि, उदाहरण के लिए, जब ९८.३% की एकाग्रता पर nachinajutperegonjat सल्फर एसिड ।और इसके विपरीत, समाधान है कि अधिक ध्यान केंद्रित कर रहे हैं, अधिक सल्फर एनहाइड्राइड वाष्पीकरण से ।३३७ डिग्री सेल्सियस एसिड आंशिक रूप से ऐसा करने के लिए विघटित के तापमान पर Parkipjashhej3 और (ज)2हे, जो जब ठंडा हो गया फिर budutsoedineny. इस अम्ल के उच्च उबलते बिंदु उपयुक्त हैअपने kislotiz लवण अत्यधिक अस्थिर जब गर्म बनाने में इसका इस्तेमाल करते हैं ।
एसिड के साथ काम करते समय सावधानियां
सल्फर एसिड के उपचार में जब मारा बेहद सतर्क होना चाहिए । त्वचा पर यह अम्ल, त्वचा सफेद हो जाती है, तब burovatoj और लालिमा दिखाई देती है.आसपास के ऊतकों जबकि प्रफुल्लित । जब आप शरीर के किसी भी हिस्से के लिए इस एसिड मारा, यह जल्दी से पानी के साथ दूर धोया जाना चाहिए, और सोडा समाधान के साथ obozhzhjonnoe जगह तेल ।
अब आप जानते है कि सल्फर एसिड जिसके गुण अच्छी तरह से शोध कर रहे हैं, केवल विविध उत्पादन और खनन के लिए अपूरणीय ।